한미약품 '관절염' 치료제 '히알루마', 미국 FDA 판매허가 획득
한미약품의 관절염 치료제 히알루마가 미국 식품의약국 시판허가를 획득했다.
 한미약품
한미약품
[인사이트] 이하린 기자 = 관절염 치료제 '히알루마' 주사제가 미국 식품의약국(FDA) 시판허가를 획득했다.
FDA는 미국 내에서 생산되는 식품, 의약품, 화장품 및 수입품, 수출품 등의 효능과 안정성을 관리하는 행정기구다.
9일 의약품 제조업체 '한미약품'은 히알루마가 국산 히알루론산 제품으로는 처음으로 미국에서 판매 허가를 받았다고 밝혔다.
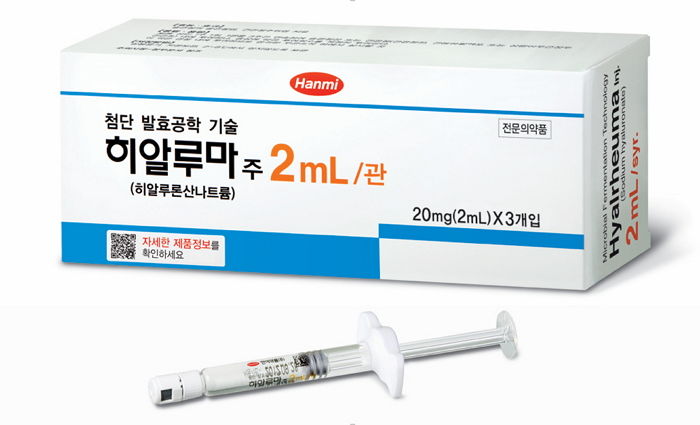
히알루마는 한미약품이 첨단 발효공학 기술을 이용해 자체 개발한 고분자 히알루론산 주사제로, 관절 내에 직접 투여하는 방식이다.
 한미약품
한미약품
한미약품은 이번 FDA 시판허가를 계기로 현지 파트너사인 '테바'와 함께 미국 전역 판매를 본격화할 예정이다.
테바는 히알루마의 미국 시판허가를 위해 미국 현지 환자 600여 명을 대상으로 임상 3상을 진행했다.
임상 3상은 다수의 사람을 대상으로 의약품 효능을 최종 점검하는 실험이며, 실질적으로 약품이 출시되기 직전 단계에서 진행한다.
한미약품은 시판허가를 받기 위한 중요한 절차인 '히알루마 생산 공장에 대한 FDA 실사'를 성공적으로 통과했다.
 한미약품
한미약품
한미약품은 당초 2014년 미국 제네릭 1위 제약기업 '악타비스'와 히알루마의 미국 수출 계약을 체결한 바 있다.
그러나 악타비스가 2016년 8월 테바에 인수합병되면서 히알루마 파트너사가 테바로 변경됐다.
한미약품 관계자는 "히알루마가 까다로운 FDA 실사를 통과해 세계 최대 의약품 시장인 미국에서 국내 최초로 시판허가를 받게 됐다"고 밝혔다.
이어 "한미약품의 기술력과 브랜드를 통해 한국을 넘어 세계인의 삶의 질을 높이는데 기여하겠다"라고 덧붙였다.